Original: http://www.tulane.edu/~wiser/protozoology/notes/malaria.html
Маларија беше и се уште е причина за многу човечка морбидитет и морталитет. Иако болеста е искоренета во повеќето умерените зони, таа продолжува да биде ендемични низ поголемиот дел од тропските и суптропските. Четириесет проценти од светската популација живее во ендемските области. Епидемија уништени големи популации и маларија претставува сериозна пречка за економскиот напредок во многу земји во развој. Постојат околу 300-500 милиони случаи на клиничката болест годишно со 1.5-2.7 милиони смртни случаи. Некои од најраните познати медицински записи од Кина, Асирија и Индија точно да ја опишуваат маларија како повремен треска. Хипократ, “татко на медицината”, генерално е заслужен првиот опис на клиничките симптоми во 500 п.н.е., повеќе од 2000 години пред паразит беше опишани (Табела). [Види исто така Википедија за историјата на маларија.]
| 500 _ п.н.е. | Хипократ | Клиничките симптоми |
| 1880 | Лаверан | Фаза на крв |
| 1898 | Рос | Пренос комарец |
| 1948 | Гернхем | Фаза на црниот дроб |
- Животен циклус
- Kлинички манифестации
- Патогенеза и церебрална маларија
- Епидемиологија и контрола
- Дијагноза
- Хемотерапијата и отпорност на лековите
Маларијата е предизвикан од членови на родот плазмодиум. Плазмодиум видови се апикомплекс (види општ опис на апикомплекс) и покажуваат heteroxenous животниот циклус вклучува ‘рбетни домаќин и вектор на членконоги. ‘Рбетни домаќини се: влечуги, птици, глодари, мајмуните и луѓето. плазмодиум видови обично се биде домаќин на специфични и вектор специфична по тоа секој вид ќе се појават само ограничен опсег на домаќините и вектори. Четири заразени различни видови на луѓето: P. фалципарум, P. vivax , P. ovale и P. маларија. (Видете на страница на разликите видови.) Видовите се разликуваат во однос на нивната морфологија, детали од нивниот животен циклус, како и нивните клинички манифестации.
Животен циклус
Човекот и други цицачи плазмодиум видови се пренесуваат преку анофелин комарци. Паразитот се вбризгува со плунката при хранење комарци и првиот подложува на круг merogony во црниот дроб проследено со повеќе рунди на merogony во еритроцитите. Гаметогони започнува во еритроцитите на ‘рбетни домаќин и да се заврши во рок од комарец споророгија каде што се одвива. Оваа животниот циклус покажува општите карактеристики на други апикомплекс паразити се карактеризира со асексуален репликација и формирање на инвазивен фази со типичен апикален органели.
Фаза на црниот дроб. Хуманата инфекција е инициран, предизвикан кога спорозоитите се вбризгува со плунката при хранење комарец. На спорозоите влезат во циркулаторниот систем и во рок од 30-60 минути ќе напаѓа клетките на црниот дроб. Домаќинот влез ќелија, како и во сите апикомплекс, е олеснета од страна на апикална органели. По освојувањето на хепатоцитите, паразитот се подложува на бесполово размножување. Ова репликациски фаза често се нарекува екзоеритроцитска шизогонија.
Шизогонија однесува на репликациски процес во кој паразитот се подложува на повеќе рунди на нуклеарна поделба без цитоплазматски поделба проследено со младиот и надежен, или сегментација, да се формира потомство. Потомство, наречен мерозоити, се ослободуваат во системот за крвоток следниве руптура на хепатоцитите домаќин. (Види живот фигура циклус.)
Во P. vivax и P. ovale некои од спорозоитите не веднаш да се подложат на асексуален репликација, но влезе во хибернација фаза позната како хипнозоит. (Сепак, некои прашања за тоа дали P. ovale експонати фаза хипнозоит биле покренати. Види Рихтер et al, 2010 година, паразитологија истражување 107:.. 1285) Ова хипнозоит може да се реактивира и се подложени шизогонија подоцна резултира со релапс. Релапс има специфично значење во однос на маларија и се однесува на реактивирање на инфекцијата преку хипнозоитs. Повторно се користи за да се опише ситуацијата во која паразитмија паѓа под забележливи нивоа, а потоа подоцна се зголемува на патент паразитмија. Интересно е тоа што видови изолирани од умерените региони имаат тенденција да ги изложат подолг латентен период помеѓу примарната инфекција и прв релапс од притисоците од тропските региони со континуиран пренос (Слика).
Фаза крв. Мерозоити ослободен од инфицираните клетки на црниот дроб нападне еритроцитите. На мерозоити препознаваат специфични протеини на површината на еритроцитите и активно инвазија на клетки на начин сличен на други апикомплексn паразити. (Види детали на механизмот на клетката на домаќинот инвазија.) По влегувањето во еритроцитите паразитот се подложува на трофични период проследен со бесполово размножување. Младиот трофозоит често се нарекува форма на прстен, поради неговата морфологија геимза дамки крв дамки. Како што се зголемува во големина паразит овој морфологија “прстен” ќе исчезне и тоа се нарекува трофозоит. За време на периодот на трофични паразит внесува клетката на домаќинот цитоплазма и се распаѓа на хемоглобинот во амино киселини. А по-производ на варење на хемоглобинот е маларија пигмент, или хемозоин. (Види забелешки за храна вакуола на плазмодиум). Овие златно-кафеава до црна гранули се одамна признати како посебна карактеристика на крв фаза паразити.
Нуклеарна поделба означува крајот на фазата на трофозоит и почетокот на шизон фаза. Еритроцитни се состои од 3-5 круга (во зависност од видот) на нуклеарна репликација проследено со младиот и надежен процес. Доцна фаза шизонти во кое индивидуата мерозоити стане видлива се нарекуваат сегменти. Раскинува домаќин на еритроцитите и изданија на мерозоити. Овие мерозоити нападне нови еритроцити и иницира уште една рунда на шизогонија. Паразити крвта фаза во рамките на домаќин обично се подложи на синхрони шизогонија. Истовремен прекин на инфицираните еритроцити и истовремена ослободување на антигени и отпадните производи сметки за наизменична пароксизам треска поврзани со маларија. Фаза на крв во шизогонија P. фалципарум се разликува од другите човечки маларичните паразити во кои трофозоит- и шизон инфицираните еритроцити се придржуваат на капиларните ендотелни клетки и не се наоѓаат во периферната циркулација. Ова секвестрација е поврзана со церебрална маларија. (Види слика живот циклус.)
Сексуална сцена. Како алтернатива на шизогонија некои од паразити ќе биде подложен на сексуална циклус и смртно се разликува во или микро или макрогаметоцити. Фактори кои се вклучени во поттикнување на гаметоцитогенеза не се познати. Сепак, посветеноста на сексуална сцена се случува за време на асексуален еритроцитни циклус кој веднаш му претходи гаметоцит формации. Ќерката мерозоити од овој шизон ќе се развие во или сите асексуален форми или сите сексуални форми. Гаметоцити не предизвикуваат патологија во човечки домаќин и ќе исчезне од циркулацијата ако не е донесена од страна на комарец.
Гаметогенеза, или формирање на микро и макрогаметы, е предизвикана кога гаметоцити се проголтан од страна на комарец. По ингестијата на комарец, на микрoгаметоцит подложува на три круга на нуклеарна репликација. Овие осум јадра потоа стана поврзани со флагели кои произлегуваат од телото на микрoгаметоцит. Овој процес е лесно да се набљудуваат на светлосна микроскопија поради флагели на пердах и се нарекува. На макрогаметоцити созреат во макрогаметы. Сепак, на морфолошки ниво ова е многу помалку драматични од изложени од страна на микрогаметоцит.
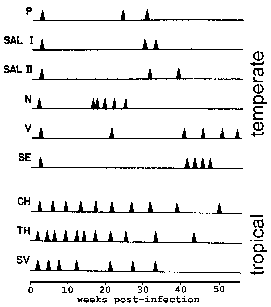 Мајмуни се следат за тајмингот на рецидиви после инфекција со различни изолати. P. vivax соеви изолирани од Америките (горниот) покажуваат “умерена” релапс шемата додека оние од југоисточна Азија (пониски) покажуваат “тропска” шемата на релапс. Изменето од Contacos et al во AJTMH 21: 707, 1972 година.
Мајмуни се следат за тајмингот на рецидиви после инфекција со различни изолати. P. vivax соеви изолирани од Америките (горниот) покажуваат “умерена” релапс шемата додека оние од југоисточна Азија (пониски) покажуваат “тропска” шемата на релапс. Изменето од Contacos et al во AJTMH 21: 707, 1972 година.
Гаметогенеза, или формирање на микро и макрогаметы, е предизвикана кога гаметоцити се проголтан од страна на комарец. По ингестијата на комарец, на microгаметоцит подложува на три круга на нуклеарна репликација. Овие осум јадра потоа стана поврзани со флагели кои произлегуваат од телото на microгаметоцит. Овој процес е лесно да се набљудуваат на светлосна микроскопија поради флагели на пердах и се нарекува ексфлагелация. На макрогаметоцити созреат во макрогаметы. Сепак, на морфолошки ниво ова е многу помалку драматични од ексфлагелация изложени од страна на микрогаметоцита.
Се случува спонтано кога инфицирана крв е изложен на воздух. Критични фактори кои се вклучени во индукција на оваа Гаметогенеза се намалување а температура, намалување на растворен јаглерод диоксид и следните зголемување на pH вредноста на 8,0 погоре (кутија). Ова донекаде мимика промените на животната средина од страна на искусни гаметоцити во кои ќе има промена на собна температура и стомакот на комарците експонати pH вредност од околу 7,8 во споредба со pH вредност од 7,4 за крв. Покрај тоа, комарец добиени ексфлагелация фактор (МЕФ) исто така е опишана и се идентификувани како xanthurenic киселина, метаболит од инсекти. Киселина ја намалува попустлив pH вредност за ексфлагелация на под 8.0 и е можеби биолошки знак за паразит да се подложат на Гаметогенеза (Billker et al, Природа 392: 289, 1998; Billker et al, 117 Мобилен: 503, 2004).
| Гаметогенеза / ексфлагелация |
|---|
|
На високо мобилни микрогамента ќе се бараат и да се спои со macrogamete. Во рок од 12-24 часа како резултат на зигот се развива во една. На окинети е подвижни инвазивен фаза која ќе попречно двете перитрофик матриксот и средината на стомакот епител на комарец. Трансверзација на средината на стомакот епител вклучува освојувањето и излегување неколку епителните клетки пред новите на базалните страна на епителот. Процесот на инвазијата е сличен на другите апикомплекс освен дека нема и не се формира паразитофорен вакуола по инвазијата на клетката на домаќинот. (Види детали на механизмот на клетката на домаќинот инвазија.)
Споророгија. По донесувањето на екстрацелуларниот простор помеѓу епителните клетки и базалната ламина, на ookinete прераснува во ооциста. Ооцистите се подложат асексуален репликација, наречен споророгија, која кулминира во производството на неколку илјади спорозоити. Ова обично трае 10-28 дена, во зависност од видот и температура. По созревање на руптура на ооциста и ослободува спорозоити кои преминуваат базалната ламина во хемокоел (телесна празнина) од комарец. (Види слика живот циклус.)
Овие спорозоити се подвижни и имаат способност да ги конкретно признае плунковните жлезди. По наоѓање на плунковните жлезди спорозоити ќе нападне и попречно на плунковна жлезда епителните клетки и да дојде да лежи во рамките на своите лумен. Некои од овие спорозоити ќе биде протеран во ‘рбетни домаќин како комарец зема крв оброк, а со тоа повторно инфекција во’ рбетни домаќин. Иако спорозоити жлезда хемокоел и плунковните се морфолошки слични, тие се функционално различни. Плунковните жлезди спорозоити ефикасно ги нападне клетките на црниот дроб, но не може повторно да нападне плунковните жлезди, додека спорозоити на хемокоел се неефикасни во освојувањето на клетките на црниот дроб.
Во краток преглед, паразитот на маларијата покажува животниот циклус со типичен апикомплексn карактеристики. Постојат три различни инвазивни фази: спорозојт, мерозојт и окинети. Се карактеризира со апикална органели и да ги нападне или да помине преку клетки домаќин. Се забележани два различни видови на мерогони. Првата, наречена екзоэритроцит шизогонија, се јавува во црниот дроб и се иницирани од страна на спорозоит. Како резултат на мерозоити потоа ги нападне еритроцитите и се подложени на повторени рунди на merogony наречен еритроцитни шизогонија. Некои од мерозоити произведени од еритроцитната шизогонија ќе бидат подложени на gamogony. Плазмодиум gamogony е опишан во две фази: гаметоцитогенеза случуваат во крвотокот на ‘рбетни домаќин, и Гаметогенеза одвива во стомакот на комарец. На полови клетки осигурач да стане зигот кој прв се развива во една ookinete и тогаш станува ооциста споророгија каде што се одвива.
(За преглед на животниот циклус во рамките на комарец види Лос Анџелес Батон, LC-Ranford Картрајт (2005) Ширење на семето на милиони убиство на смртта. Метаморфози на маларија во комарец Трендови во паразитологија 21, 573-580.)
Клинички манифестации
Патологија и клинички манифестации поврзани со маларија се речиси исклучиво се должи на асексуален еритроцитната фаза паразити. Ткиво шизонти и гаметоцити предизвика малку, доколку ги има, патологија. Плазмодиум инфекцијата предизвикува акутна фебрилна болест која е најмногу познат по својата периодични пароксизам треска се случуваат на или 48 или 72 интервали час. Тежината на нападот зависи од плазмодиум видови, како и други околности, како што се состојбата на имунитетот и општо здравје и исхрана на заразено лице. Маларијата е хронична болест која има тенденција да се релапс (види објаснување на разликата), со месеци или дури со години.
Највообичаен начин да се добие маларија е преку природен пренос од комарци (види животниот циклус). Маларија, исто така може да се пренесе преку трансфузија на крв или споделување шприцеви. Механички пренос на заразена крв ќе резултира со пократок период на инкубација, бидејќи нема да има на црниот дроб фаза. Исто така, постои зголемен ризик на смртност со механичко-преносливи P. фалципарум. На недостаток на инфекција на црниот дроб фаза, исто така, го спречува релапси во P. vivax или P. ovale инфекции. Вродени пренос, исто така, биле документирани, но се верува дека се релативно ретки и покрај тешка инфекција на плацентата.
Екзоэритроцит шизогонија и препатент и периоди на инкубација
|
P. фалципарум
|
P. vivax
|
P. ovale
|
P. маларија
|
|
| препатент период (денови) |
6-9
|
8-12
|
10-14
|
15-18
|
| Инкубација период (денови) |
7-14
|
12-17
|
16-18
|
18-40
|
| мерозоит созревање (дена) |
5-7
|
6-8
|
9
|
12-16
|
| мерозоити произведени |
40.000
|
10.000
|
15.000
|
2000
|
Симптоми на маларија обично почнуваат да се појавуваат 10-15 дена по каснување од заразено од комарец. Типичен препатент и периоди на инкубација следниве спорозоит инокулација се разликуваат според видови (Табела). На препатент период е дефиниран како време помеѓу спорозоит инокулација и појавата на паразити во крвта и го претставува времетраењето на фазата на црниот дроб и бројот на мерозоити произведени. Инкубацијата периоди имаат тенденција да бидат малку подолго и се дефинира како време помеѓу спорозоит инокулација и почетокот на симптомите. Понекогаш периодот на инкубација може да се пролонгира за неколку месеци во P. vivax, P. ovale, и P. маларија. Сите четири видови можат да покажуваат неспецифични продромални симптоми неколку дена пред првиот febril напад. Овие продромални симптоми обично се опишува како “слични на грип и вклучуваат: главоболка, малку покачена температура, болки во мускулите, анорексија, гадење и замор. Симптомите имаат тенденција да се поврзе со зголемување на бројот на паразити.
Овие продромални симптоми ќе биде проследена со фебрилни напади исто така познат како на маларијата пароксизам. Овие пароксизам ќе ги изложат периодичноста од 48 часа за P. vivax, P. ovale и P. фалципарум, и 72-часовен поените за P. маларија. Првично периодичноста на овие paroxyms може да биде неправилна како легла на мерозоити од различни екзоэритроцит шизонти синхронизирате. Ова е особено точно во P. фалципарум, кои не можат да покажуваат различни пароксизам, но покажуваат континуиран треска, дневни напади или неправилни напади (на пр., 36-48 часа периодика). Пациентите може исто така покажуваат спленомегалија, хепатомегалија (мало жолтица), и хемолитична анемија за време на периодот во кој се случи пароксизам на маларија.
На маларијата пароксизам
| Ладно фаза | Жешка сцена | Потење фаза |
|
|
|
На маларијата пароксизам (види Табела) ќе обично траат 4-8 часа и почнува со ненадејна појава на треска во која пациентот доживува интензивно чувство на ладно и покрај тоа што покачена температура. Ова често се нарекува како ладна фаза и се карактеризира со силен грч. Веднаш по ова ладно фаза е жешка сцена. Пациентот се чувствува интензивна топлина придружена со силна главоболка. Замор, вртоглавица, анорексија, болки во мускулите, гадење и често ќе бидат поврзани со жешка сцена. Следен период од профузно потење ќе последвам и треската ќе почне да се намалува. Пациентот е исцрпена и слаба и обично ќе заспие. По будењето на пациентот обично се чувствува добро, освен да биде уморен, и не покажуваат симптоми до почетокот на следниот пароксизам.
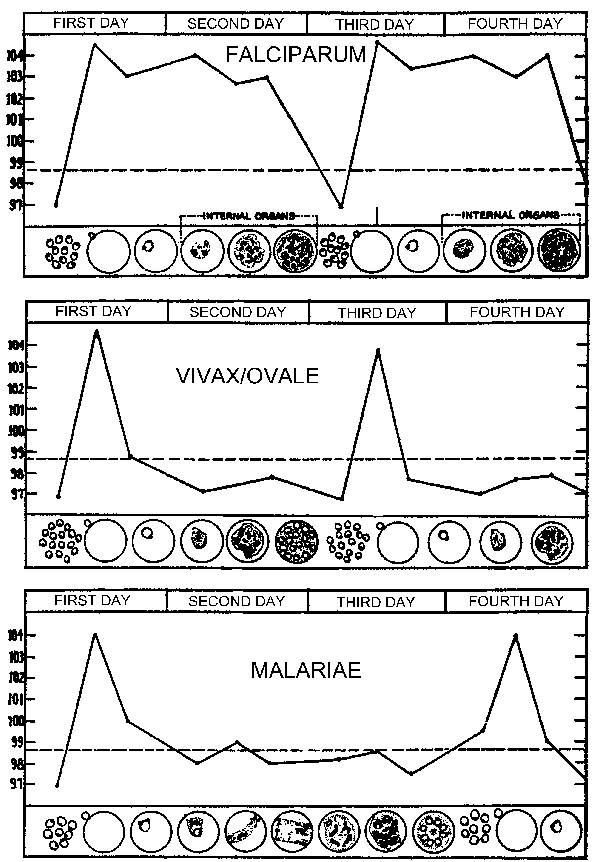
А типичен модел на температура (треска) во однос на крв-фаза шизогонија за човечкиот маларични паразити. paroxysm На треска одговара на периодот на инфицираните еритроцити руптура и мерозоит инвазија. (Слика изменета од Нева и Браун, основни клинички паразитологија, 6-ти ед., 1994)
Периодичноста на овие пароксизми се должи на синхрони развој на паразитот на маларијата во човечки домаќин. Со други зборови, сите паразити во рамките на домаќин се на приближно иста сцена (на пример, прстен, трофозоит, шизон), како тие се продолжи преку шизогонија. На маларични paroxysm одговара на руптура на инфицираните еритроцити и ослободување на мерозоити (Слика погоре). 72 часа периодичноста во P. маларија се должи на неговата побавен раст и созревање за време на крв-фаза шизогонија. Студии во P. vivax покажаа корелација помеѓу треска и серум TNF-α (тумор некроза фактор-алфа) нивоа (слика десно). Веројатно антигени или токсини се ослободуваат кога инфицирани еритроцитна руптура и да доведе до производство на TNF-α и фебрилни напади.
Тежината на пароксизмите и времетраењето на симптомите варира во зависност од видот (види табела подолу). Во принцип, сериозноста на болеста во корелација со просечна и максимална паразитмија изложени од страна на различни видови. P. фалципарум е способен за производство на тешка и смртоносна инфекција, додека други видови се ретко смртник. Пациентите инфицирани со P. vivax, особено за прв пат, може да биде прилично болен. Сепак, P. vivax ретко предизвикува компликации или резултира со смрт. На повод тешка маларија вклучуваат повеќе органи, исто така, е забележано во P. vivax инфекции (види Kochar et al, Еид 11 (1), јануари 2005 година).Релапсите до активирање на P. vivax хипнозоитs може да се случи за неколку години. P. ovale е најстариот бенигни во кои пароксизмите имаат тенденција да бидат благи и траат кратко и рецидиви ретко се случуваат повеќе од една година по првичната инфекција. P. маларија обично произведува лесна болест, но првичната пароксизам може да биде умерена до тешка. Тоа е најмногу хронична, иако, и повторноs биле документирани неколку децении по првичната инфекција. Оваа хроницитет понекогаш е поврзан со бубрежни компликации, кои веројатно се резултат на таложење на антиген-антитело комплекси во гломерулите на бубрегот. На маларијата пароксизам ќе стане помалку тешки и неправилна периодичноста како домаќин развива имунитет. Oва имунитет Меѓутоа, не е стерилизирање имунитет дека инфекцијата трае подолго од симптомите и физички лица можат да покажат релапси или повторноs или да стане реинфекција. Ако не се лекува, сите форми на маларија имаат тенденција да бидат хронични.
 Температурата на телото (кругови) и нивоата на TNF (триаголници) се мери во текот на маларијата пароксизам. Црната кутија означува периодот на интензивна треска и отворена кутија означува профузно потење. Изменето од Karunaweera et al (1992) proc. NATL. Акад. Сци. 89: 3200 .
Температурата на телото (кругови) и нивоата на TNF (триаголници) се мери во текот на маларијата пароксизам. Црната кутија означува периодот на интензивна треска и отворена кутија означува профузно потење. Изменето од Karunaweera et al (1992) proc. NATL. Акад. Сци. 89: 3200 .
| vivax | ovale | маларија | фалципарум | |
|---|---|---|---|---|
| Почетна Paraoxysm Сериозност | умерена до тешка | благи | умерена до тешка | тешка |
| Просечна паразитмија (mm 3 ) | 20.000 | 9.000 | 6.000 | 50,000-500,000 |
| Максимална паразитмија (mm 3 ) | 50.000 | 30.000 | 20.000 | 2,500,000 |
| Симптом Времетраење (нетретирани) | + 3-8 недели | 2-3 недели | 3-24 недели | 2-3 недели |
| Максимална Инфекција Времетраење (нетретирани) | 5-8 години | 12-20 месеци | 20-50 + години | 6-17 месеци |
| анемија | ++ | + | ++ | ++++ |
| компликации | бубрежна | церебрална | ||
| Изменето од Markell и Voge Медицински паразитологија | ||||
| Зголемен морбидитет и морталитет од фалципарум маларија |
|---|
|
За разлика од другите три видови, P. фалципарум може да произведе сериозни болест со смртни последици. Овој зголемен морбидитет и морталитет делумно се должи на високата паразитмијаs поврзани со P. фалципарум инфекции. Овие потенцијално висока паразитмијаs се должи делумно на големиот број на мерозоити произведени и способноста на P. фалципарум да ги нападне сите еритроцитите. Спротивно на тоа, P. vivax и P. ovale преферираат ретикулоцитите (на пример, незрели еритроцити), додека P. маларија сака senescent еритроцитите (види разликите видови). На паразитмија може исто така брзо се зголеми како резултат на цитоадхеренција и конфискување на P. фалципарум. Ова секвестрација во ткивата минимизира отстранување на заразените еритроцити од страна на слезината и овозможува поефикасна еритроцитите инвазија. Високата паразитмија и секвестрација резултат во други компликации поврзани со фалципарум маларија, најзначајните се анемија и церебрална маларија (дискутирани во следниот дел). Анемијата се должи во дел до уништување на еритроцити за време на крв-фаза шизогонија. Исто така, не-инфицирани еритроцитите се уништени на повисоки стапки за време на инфекцијата и таму е намалена продукција на еритроцити.
Патогенеза и тешка маларија
Патологија поврзана со сите видови маларијата е поврзана со прекин на заразени еритроцити и ослободување на паразитот материјал и метаболити, хемозоин (на пример, маларија пигмент) и мобилните остатоци. Во прилог на дискутирано погоре пароксизам, таложење на хемозоин одамна е познат како карактеристика на маларија. Постои зголемена активност на ретикулоендотелниот систем, особено во црниот дроб и слезината и на тој начин нивната проширување, како што беше потврдено од страна на макрофагите со проголтан заразени и нормална еритроцити и хемозоин. Освен за P. фалципарум, што патолошките појави поврзани со маларија има тенденција да биде бенигно. Неколку тешки компликации може да биде поврзан со фалципарум маларија со церебрална маларија се најзначајните и честа причина за смрт.
| церебрална маларија |
|---|
|
Церебрална маларија се карактеризира со нарушена свест (кутија). Презентирачки симптоми се тешки главоболки проследено со поспаност, збунетост, и на крајот кома. Конвулзиите се, исто така, често се поврзани со церебрална маларија. Овие невролошки манифестации се верува дека се должи на изолирање на инфицираните еритроцити во церебралниот микроциркулацијата. Секвестрација однесува на цитоадхеренција на трофозоит- и шизон инфицираните еритроцити за ендотелните клетки на длабока васкуларни легла во виталните органи, особено мозокот, белите дробови, стомакот, срцето и плацентата. Ова секвестрација нуди неколку предности за паразит. На голема предност е избегнување на слезината, а потоа и отстранување на инфицирани еритроцитите. Покрај тоа, ниско ниво на кислород тензии во длабоките ткива може да се обезбеди подобра метаболна средина.
Цитоадхеренција се чини дека со посредство на електронски густи избувнувања на површината на инфицираните еритроцити. Овие “копчиња” се изразени во текот на фазите на трофозоит и шизон и се формираат како резултат на паразит протеини извезуваат на еритроцитната мембрана. Меѓу човечките плазмодиум видови, копчиња се ограничени на P. фалципарум и на тој начин укажуваат на тоа дека рачки играат улога во цитоадхеренција. Покрај тоа, таму е исто така добра корелација помеѓу животните плазмодиум видови кои изразуваат копчиња и изложба секвестрација. Електронска микроскопија, исто така, покажува дека рачки се контактирање помеѓу заразените еритроцити и ендотелните клетки.
Молекуларните механизми на цитоадхеренција вклучуваат рецептор-лиганд интеракции. Со други зборови, протеини, изразени на површината на инфицираните еритроцити (лиганд) ќе се поврзе со протеини изразени на површината на ендотелните клетки (рецептор). Pf EMP-1 (e еритроцит m мембрана p протеин) е паразит протеин кој е вмешан како цитоадхеренција лиганд (кутија). Во контраст на обично високо конзервирани природата на рецептор-лиганд интеракции, Pf EMP-1 е член на високо променлива (= var) Ген семејство со 40-50 различни гени. Неколку домаќин протеини кои можеби функционира како што се идентификувани рецептори (види полето подолу). Многу од овие домаќин протеини функционира во клетка-клетка интеракциите и се вклучени во клеточната адхезија. Неколку студии покажуваат дека изразувањето на различните Pf EMP-1 гени е во корелација со различни рецептор-врзувачкиот фенотипови. Ова антигенски варијации поврзани со површина изложени Pf EMP-1 му овозможува на паразит да се избегне имунолошкиот систем. Меѓутоа, функцијата на цитоадхеренција е зачувана преку неговата способност да ги препознае повеќе рецептори (Слика). Ова антигенски варијации исто така може да сметка за различни исходи болест. На пример, меѓуклеточната адхезивна молекула-1 (ICAM-1) обично се вмешани во церебралната патологија.
| Pf EMP-1 |
|---|
|
| можни рецептори |
|---|
|
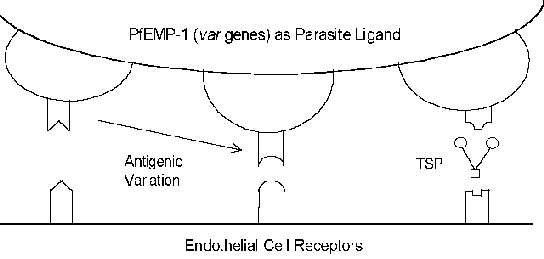
Кликнете тука за повеќе информации за рачки, рецептори/лиганди, и антигенски варијации.
Почетокот на набљудувања на патологијата на церебрална маларија предложи врска помеѓу голем број на заразени еритроцити во микроциркулацијата и развој на синдромот. Првично се претпоставуваше дека цитоадхеренција ќе доведе до блокада механички (на пример, церебрална исхемија) а потоа и хипоксија. Покрај тоа, на паразит исто така, може да предизвика локализиран метаболни ефекти како што се хипогликемија и/или лактична ацидоза. Тогаш хипоксија и метаболни ефекти ќе предизвика кома и последователна смрт. Сепак, постојат некои проблеми со хипотезата за врзување на:
- кома поврзана со церебрална маларија е брзо реверзибилни по третман,
- висок процент на преживеани немаат постојан невролошки компликации,
- недостаток на исхемично оштетување (ја отфрли можноста хипоксија како главен механизам),
- секвестрација, исто така, се јавува во не-церебрална маларија.
Невролошки секвели меѓу преживеаните од церебрална маларија:
ван Hansbroek (1997) Ј PED. 131: 125 |
Поради овие проблеми други сугерираат дека кома е посредувана од краткотрајна молекули кои влијаат церебрална функција. Можно медијатори домаќин вклучуваат цитокини, како што TNF- на, или азотен оксид. Во оваа теорија на цитокини, маларичен антигени ќе го стимулира TNF- на кои потоа би можеле да предизвикаат азотен оксид или има и други патолошки ефекти. Азотниот оксид е познато дека влијае на невронската функција и тоа би можело да доведе до интракранијална хипертензија преку своите вазодилататор активност. Тоа е малку веројатно, сепак, дека системски ослободување на цитокини ќе предизвика кома и треба да се, исто така претпоставуваат дека ослободувањето на медијаторите во мозокот ќе доведе до високи локални концентрации. Покрај тоа, има минимални лимфоцитна инфилтрација или воспаление поврзани со блокирани капилари.
Хипотезата за секвестрација и теорија цитокин за патофизиологијата на церебрална маларија меѓусебно не се исклучуваат, и двете феномен, најверојатно, ќе бидат вклучени. На пример, паразит exo-антигени, кои се објавени на еритроцитите прекин, се познати да се стимулираат макрофагите да TNF- лачат еден. TNF- на е познато да изразување на адхезија молекули, како што ICAM-1 на површината на мозокот ендотелијалните клетки. Ова ќе доведе до зголемување на врзување на инфицираните еритроцити и засилување на ефектите дали тие се резултат на васкуларна блокада, растворливи медијатори, метаболни ефекти, или комбинација (слика).
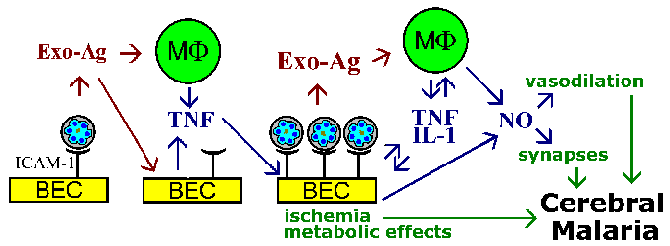
Шематски модел е претставен некои можни медијатори на церебрална маларија. На цитоадхеренција на инфицираните еритроцити на мозокот ендотелијалните клетки (BEC) и ослободување на exo-антигени може да го стимулира BEC и имунолошкиот ефекторни клетки таков макрофаги (М F ) за да се лачат цитокини. Овие цитокини, како што се тумор некроза фактор- a (TNF), ќе доведе до зголемена експресија на можни ендотелијална клеточна рецептори (на пр., ICAM-1) и да се промовира зголемување цитоадхеренција на инфицираните еритроцити. Голем број на обврзана заразени еритроцити може да доведе до васкуларна блокада и хипоксија и се локализирани метаболички ефекти (на пр., Хипогликемија, млечна ацидоза).Зголемениот број на заразени еритроцити и exo-антигени, исто така, ќе доведе до повисоки нивоа на цитокини. TNF- на е познат, исто така, да се стимулира азотен оксид (NO). Азотниот оксид може да влијае на невронската функција од мешање со невротрансмисијата. Азотниот оксид, исто така, предизвикува вазодилатација која може да доведе до интракранијална хипертензија поврзана со церебрална маларија. Слика адаптирана од Pasloske и Хауард (Отк Annu Мед 45:.. 283, 1994).
Во краток преглед:
- P. фалципарум може да предизвика тешка и смртоносна болест
- тоа се зголеми pathogenecity во споредба со другите човечки маларија е поврзана со P. фалципарум е:
- високо репродуктивна способност
- цитоадхеренција и секвестрација
- секвестрација придонесува за повисока репродуктивна способност преку избегнување на слезината
- на цитоадхеренција на ендотелните клетки, исто така, би можеле да имаат локални патолошки ефекти, а особено е најверојатно се вклучени во церебрална маларија
- патофизиологијата на церебрална маларија не е целосно сфатена, но веројатно вклучува повеќе фактори и комплексни интеракции помеѓу домаќинот и паразитот
Критика на тешка маларија и патогенеза:
- IA Кларк, СБ Cowden (2003) патофизиологијата на фалципарум маларија. Фармакологија и терапевтика 99, 221-260.
- Idro R, NE Џенкинс, CRJC Њутн (2005) патогенезата, клиничката слика и невролошки исход од церебрална маларија. The Lancet неврологија 4, 827-840.
- CL Мекинтош, JG Beeson, К Марш (2004) Клинички карактеристики и патогенезата на тешка маларија. Трендови во паразитологија 20, 597-603.
- А Trampuz, М Jereb, јас Muzlovic, РМ Prabhu (2003) Клинички преглед: Тешка маларија. Интензивна нега 7, 315-323.
Епидемиологија
Одете во делот за: Маларијата е првенствено болест на тропските и суптропските и е широко распространета во топла влажна региони на Африка, Азија и Јужна и Централна Америка. Оваа болест е исто така честа појава во многу умерените области, вклучувајќи ги САД, Европа и северниот дел на Евроазија и Азија, но е искоренета.Во многу области кои претходно имаа маларија под контрола се доживува препород (види статија во The Atlantic). На четири човечки маларијата видови покажуваат преклопување географска дистрибуција (Табела). P. vivax и P. фалципарум се најчесто се среќаваат видови со P. vivax се најраспространети географски. Мешани инфекции се чести во ендемските области. Молекуларни методи укажуваат на тоа дека P. маларија и P. ovale може да биде повеќе широко распространета и распространети што претходно се мислеше (види Милер et al, Tr Parasitol 23:.. 278 , 2007).
Географската распределба
vivax
фалципарум
маларија
овале
- широко распространета во тропските и суптропските области
- спектар се протега во умерените области
- релативно ретки во Африка
- широко распространета, но пред се во тропските и суптропските
- широка, но петна географска дистрибуција
- пред тропска Африка, особено во западниот брег
| маларија епидемиологија |
|---|
стабилна или ендемични маларија
нестабилен или епидемија на маларија
|
Епидемиологија на маларија може да се гледа во однос на се стабилни (или ендемични) или нестабилна (или епидемија). Стабилна маларија се однесува на ситуација во која постои мерливо инциденцата на природен пренос во текот на неколку години. Ова исто така ќе вклучува области кои се доживее сезонски пренос. Различни области може да се доживее различни нивоа на стапките на инциденца и ова е често означена со: хипоендемичен, мезоендемичен, хипердемичен и холоендемичен. Лица кои живеат во многу ендемични области обично покажуваат високо ниво на имунитет и толерира инфекција.
Нестабилен, или епидемија, маларија се однесува на зголемување на маларија во области на ниска ендемичност или на епидемии во области претходно без маларија или меѓу не-имунолошки лица. Овие епидемии обично може да се припише на промените во однесувањето на човекот или ефекти врз животната средина. На пример, човечки миграција и раселување или може да се воведе маларија во една област или се изложуваат на претходно не се имуни на населението во ендемски пренос. Промени во областа на екологијата предизвикани од природни катастрофи или проекти за јавни работи, како што се изградба на патишта, исто така може да влијае на пренос на маларија и да доведе до епидемии.
“Сè за маларија е толку моделирана од локалните услови што станува илјада епидемиолошки загатки.” Хакет (1937)
Горенаведените цитат нагласува комплексноста на маларија и на многу аспекти експонати на болеста. Различните заедници ќе ја доживее различни маларија и, следствено, различни стратегии за контрола и третман може да биде потребно. Сложена интеракција помеѓу домаќин, паразит и вектор се главните фактори во овој епидемиолошката комплексност.
На пример, како и со сите вектор преносливи болести, паразити мора да бидат способни да се воспостави хронична инфекција во рамките на домаќин за да се зголеми можности за пренесување.Ова е особено точно во случај на сезонски пренос и во области на ниска ендемичност. И воопшто маларија инфекции се карактеризираат со почетна акутна фаза проследено со подолг релативно асимптоматски хронична фаза. Ова делумно се должи на способноста на паразит да се избегне целосно расчистување на имунолошкиот систем. На пример, P. фалципарум експонати на антигенски варијации што му овозможува да остане еден чекор понапред од имунолошкиот систем. Покрај тоа, P. vivax и P. ovale покажуваат фаза хипнозоит и се способни за релапси. Ова им овозможува на паразит да се задржи на инфекција во човечки домаќин дури и по фаза на инфекцијата во крвта е расчистено. Релативната долг интервал помеѓу релапси во некои P. vivax изолира веројатно ја објаснува неговата способност да се задржи циклуси пренос во некои умерена клима.
Неколку студии молекуларната епидемиологија посочија дека P. фалципарум, исто така, може да произведе долгорочни хронични инфекции (види Roper et al подолу).
Roper et al (1996) AJTMH 54: 32
|
| датум Тестирано |
% Инциденца (размаска / PCR) * |
||||||
|
|
} | 33% пријавиле симптоми | ||||
|
|
} | не симптоматски случаи | ||||
| * Број на лица позитивниот тест преку крвта тест и PCR. Анализа на PCR детектира ~ 2,5 паразити / m l (4-10X повеќе чувствителни отколку дебела тестови). | |||||||
Во однос на домаќинот, луѓето се единствените значајни резервоар за паразитот и одржлива пренос зависи од одржувањето на редот на инфицирани лица и контакт меѓу луѓето и анофелин комарци. Неколку фактори влијаат на осетливоста на луѓето на инфекција. Очигледно имунолошкиот статус на поединецот и на претходното искуство со маларија ќе влијае на текот на инфекцијата. Бремените жени, особено за време на првата бременост, се повеќе подложни на фалципарум маларија, како што е илустрирано од страна на повисока преваленца на инфекцијата и повисоки паразитмијаs. Покрај тоа, одредени генетски болести и полиморфизми се поврзани со намалување на инфекција или болест (види вродена отпорност).
Потенцијалот на комарците да им служи како вектор зависи од способноста за поддршка споророгија, комарец изобилство, и контакт со луѓето, кои сите се под влијание на климатските и еколошките фактори (Табела). Способноста да го поддржат споророгија е во голема мера зависи од видовите во тоа што не сите видови на Anopheles се подложни на плазмодиум инфекција. Температура и комарец долговечноста се другите клучни фактори кои влијаат врз интеракцијата на паразитот со вектор. Развој на P. фалципарум бара минимум на температура од 20 o C, со оглед на тоа минимална температура за други видови е 16 oC. Температура, исто така, влијае на времето на развој со тоа што времетраењето на споророгија е значително пократок на повисоки температури. Пократко траење на споророгија зголемува шансите дека комарецот ќе ја пренесат инфекцијата во својот животен век.
Фактори кои влијаат на векторски капацитет
споророгија |
комарец Густина |
човечки Контакт |
|
|
|
Густина комарци и исхрана навики, исто така, влијае на преносот на маларија. густина на комарец е под влијание на температурата, надморска височина, врнежи од дожд и достапноста на одгледување места, додека контакт со луѓе комарци ќе биде под влијание на однесувањето на комарец. На пример, степенот до кој одредени видови комарец е антропофилен ќе влијае на веројатноста на комарците да станат инфицирани, а потоа пренесување на инфекцијата на друг човек. Овие антропофилен тенденции се нужно апсолутно во која многу зоофилични комарци ќе се префрлат на луѓето ако густини се постигне високо ниво или користи извор на животните е намалена. склопот на време на хранење и дали комарец храни претежно во затворени простории или на отворено ќе влијае на динамиката на пренос. На пример, отворен комарци исхрана се со поголема веројатност да се најде човечка крв оброк во раните вечерните часови од оние хранење доцна во ноќта, кога повеќето луѓе се внатре. Однесувањето на комарец исто така, треба да се смета во контролни активности.
| “Парадоксално, ризиците од тешка болест во детството биле најниски меѓу популациите со најголем интензитет на пренос, а биле забележани највисоките ризици болест кај популации изложени на ниски до умерена интензитет на пренос.”
Снег et al (1997) Лансет 349: 1650 |
Имунитет
Лица кои живеат во ендемски области не се развие имунитет против маларија. Речиси секогаш некој ќе ги изложат симптоми за време на нивната почетна изложеност на маларија. Симптоми поврзани со последователните изложеноста на маларија обично се помалку сериозни, иако. На имунитет против маларијата е бавно да се развие и да се бара повеќе изложеност. Во многу ендемични области само мали деца се изложени на висок ризик за развој на тешка фалципарум маларија додека постарите деца и возрасни во суштина се заштитени од тешка болест и смрт. Сепак, ова не е имунитет стерилизирање имунитет во кои лица се уште можат да се инфицираат. Во прилог на имунитет е краток живееле и во отсуство на повтори изложеност на ниво на имунитет се намалува. На пример, претходно полу-имунолошки возрасните често ќе развијат тешка маларија по враќањето во ендемска област, откако беше во не-ендемични области за 1-2 години. Оваа состојба на делумна имунитет во која паразитмија е намален, но не се елиминира, и паразитмија се толерира подобро (Слика) понекогаш се нарекува како навреда. Навреда однесува на имунитет што е контингент на патогенот се присутни.
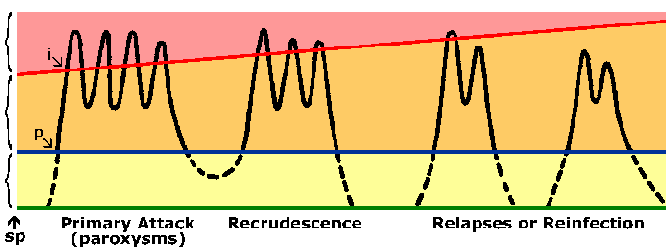
| Дијаграм претставува текот на маларија инфекција. Црна линија отсликува паразитмија крв-фаза по спорозоит инфекција (СП). Постои препатент период (P) помеѓу спорозоит инокулација и откривање на паразити во крвта. Сината линија отсликува микроскопски праг (односно, граница на детекција) и жолтата област претставува подпатент паразитмија. Портокал област претставува асимптоматски патент паразитмија.Црвената линија ја отсликува клинички праг, или паразитмија која произведува пароксизам или други клинички симптоми (розова област). Како што се развива имунитет оваа клиничка прагот се зголемува. период на инкубација (i) е време помеѓу инфекцијата и појавата на симптомите. |
Имунолошкиот одговор може да бидат насочени во било пред-еритроцитни или еритроцитни фази на животниот циклус на паразитот. Сепак, еритроцитната фаза од животниот циклус е веројатно најважниот аспект на расчистување на паразит и намалување на болеста. Поради недостаток на ХЛА молекули на површината на паразитот или еритроцити тоа е обично претпоставува дека антителата ќе игра клучна улога во крвта фаза имунитет. Можни механизми ефект за антитела вклучуваат: блокирање на еритроцитите инвазија од страна на мерозоити, антитело-зависна клеточна убивање со посредство на цитофилен антитела, или зголемен клиренс на инфицираните еритроцити се должи на врзувањето на антитела на паразитни антигени кои се изложени на површината на еритроцитите. Сите овие ќе резултира со пониски паразитмија. Релативната важност на овие различни механизми не е јасно и веројатно имунитет веројатно бара производство на антитела против голем број цели. Ова, заедно со антигенски варијација и полиморфизми во многу плазмодиум антигени, може да се објасни бавниот развој на имунитетот.
Опсервацијата дека асимптоматски индивидуи можат да покажат високо ниво на паразитмија доведе до концептот на “имунитет против болеста. Ова ќе биде во прилог на “анти-паразит имунитет дискутирано погоре што резултира со пониски паразитмијаs. Тешка маларија и смртта се во корелација со TNF-α и други проинфламаторни цитокини. Како што беше дискутирано за пароксизми и церебрална маларија, антигени или токсини објавени од страна на инфицираните еритроцити може да се стимулира производството на проинфламаторни цитокини.Антитела против овие exo-антигени би можел да го неутрализира нивните токсични ефекти и тоа да доведе до имунитет против болеста.
Преглед на имунитет на маларија:
J Langhorne, Ndungu FM, AM Sponaas, К Марш (2008) Отпорност на маларија: повеќе прашања отколку одговори. Природата имунологија 9, 725 – 732.
Поради тешкотии во контролирање на маларијата со други средства, постои голем интерес за развој на вакцина против маларија. Во моментов не постои достапна вакцина, но постои голем истражувачки напори насочени кон идентификување на вакцината кандидати и тестирање на потенцијални вакцини за безбедност и ефикасност. Комплексни животниот циклус и биологијата на паразитот обезбеди неколку потенцијални цели (Табела 15.9). На пример, вакцинирање против спорозоит или екзоэритроцит фаза може да се спречи инфекцијата. Сепак, предизвикана имунитет ќе треба да бидат целосно ефективни од бегство на еден спорозоит ќе доведе до крв фаза инфекција и болест. Вакцини насочени против мерозоити или заразени еритроцити ќе ги намали паразитмија од мешање со мерозоит инвазија или зголемување на отстранување на инфицирани еритроцитите. Таква вакцина потенцијално би можеле да се олесни многу на патогенезата поврзани со маларија, дури и ако тоа не се заврши ефикасно. Покрај тоа, инфекцијата може да служи за зајакнување на имунолошкиот одговор. Тоа може да биде можно да се вакцинираат против оваа болест со имунизација против потенцијално токсични антигени. Антителата неутрализирање антигени, кои го стимулираат имунолошкиот одговор проинфламаторни може да се намали некои од патогенезата поврзани со маларија. Исто така може да бидат насочени Сексуална фази на паразитот, како што гаметоцити и гамети. Антитела насочени против гамети антигени може да се спречи инфекција на комарци и споророгија. Таква вакцина ќе биде алтруистички во тоа што не ќе ги заштити поединецот од болеста, но се заштитат другите во заедницата, со намалување на пренос.
Потенцијални Вакцина Стратегии
| Цел | Заштита | Механизам |
| спорозоит | анти-инфекција | спречување или елиминирање на црниот дроб фаза |
| мерозоит | анти-паразит | се намали ефикасноста на мерозоит инвазија |
| инфицирани РБЦ | анти-паразит | зголемување на клиренсот на заразени еритроцити |
| екзоантиген | анти-болест | пониско производство на инфламаторните цитокини |
| сексуални сцени | анти-пренос | елиминира гамети или да се спречи инфекција од комарци |
| вродена отпорност |
|---|
|
Хумана генетика и вродена отпорност
Одредени генетски болести и полиморфизми се поврзани со намалување на инфекција или заболување (кутија). На пример, лица кои немаат крвна група антиген Дафи се отпорни на P. vivax . Голем дел од населението во Западна Африка се Дафи негативна, со што придонесуваат за ниското ниво на P. vivax во Западна Африка. Оваа вродена отпорност доведе до идентификација на антигенот Дафи како на еритроцитите рецептор за мерозоит инвазија. (Види рецептор-лиганд интеракции за време на мерозоит инвазија.)
Неколку наследни нарушувања на еритроцитите се наоѓаат претежно во маларија ендемски области и на фреквенции многу повисоки отколку што се очекуваше. Ова доведе до шпекулации дека овие нарушувања даваат извесна заштита против маларија. На пример, Југоисточна Азија овалцитоза се должи на мутација на еритроцитите мембрана протеин, наречен бенд 3. Оваа мутација предизвикува еритроцитната мембрана да станат цврсти и повеќе отпорни на мерозоит инвазија. Механизмот (и) со кои други болести може да се состане заштита од маларија не се познати. Во повеќето случаи тоа се претпоставува или шпекулира дека комбинацијата на дефектот и инфекција доведува до предвремено лиза или царинење на инфицираните еритроцити. На пример, глукоза-6-фосфат дехидрогеназа (G6PD) дефицит на еритроцити ќе имаат нарушена способност да се справи со оксидативен стрес (види Дрога акција). Дополнителните оксиданти произведени како резултат на паразит метаболизмот и варењето на хемоглобинот (види биохемија Белешки) може да победат на заразените еритроцити и да доведе до негово уништување пред паразит е во можност да ја заврши шизогонија. Српеста анемија и таласемија, исто така, се шпекулира да се направи инфицирани еритроцитите се повеќе подложни на оксидативен стрес.
Критика на црвени крвни клетки полиморфизми и маларија:
- G Мин-Oo, P Грос (2005) еритроцити варијанти и природата на нивната маларија заштитен ефект. Мобилни микробиологија 7, 753-763 .
- Тенеси Вилијамс (2006) човековите крвни клетки полиморфизми и маларија црвено. Тековни мислење во микробиологија 9, 388-394 .
- Тенеси Вилијамс (2006) клеточни дефекти на црвените крвни и маларија. Молекуларна и паразитологија Биохемиска 149, 121-127 .
| Фактори кои водат до пад на пренос на маларија во САД |
|---|
|
Маларија претходно беше повеќе распространет во умерените области, вклучувајќи Северна Америка и Европа. Се верува дека маларијата е воведен во Америка од страна на европските колонисти (P. vivax и P. маларија) и африканските робови (P. фалципарум) Во текот на 16 и 17 век. Маларија стана ендемична во многу делови на САД со исклучок на пустините и планинските области и инциденцата најверојатно достигна својот врв околу 1875 Промена на населението од руралните кон урбаните средини, одводнување на мочуришта да се создаде обработливо земјиште, подобрување на домувањето и исхраната, подобра социо-економски услови и стандарди на живеење, поголем пристап до здравствени услуги, како и достапноста на кинин за третман на сите придонесе за пад на преваленцата на маларија дури и пред воведувањето на посебни мерки (кутија). Некои контролни активности, како што се откривање на случајот и третман, и куќа прскање, беа воведени во текот на 1940-тите, и доведе до искоренување на маларија во САД. Од 1950-тите биле увезени речиси сите случаи на маларија во САД.
Огромното мнозинство на маларија случаи дијагностицирани во САД се стекнува од лица при патување во земјите каде маларијата е ендемска. Сепак, во текот на 1990-тите години имаше неколку епидемии на автохтони пренос на маларија во САД (Zucker, 1996). Овие епидемии биле поврзани со густо населените области и голем број на имигранти. Повеќе од 80% од случаите беа P. vivax . Покрај тоа, епидемии биле поврзани со невообичаено топло и влажно време, што може да го зголеми опстанок анофелин и намалување на времетраењето на sporogonic циклус, со што се овозможува за развој на инфективни спорозоити. (Види исто така неодамнешниот извештај за седум случаи на локално стекнати P. vivax маларија што се случи во Флорида во текот на јули-август 2003 година, MMWR 52: 908).
намали контакт со луѓе комарци
намалување на вектор густина
намалување на паразит резервоар
|
Pевенција и контрола
Стратегии за спречување и контрола на маларијата вклучуваат три различни пристапи (види рамка). Превенција на маларија во поединци генерално ќе вклучуваат намалување на контакт со луѓе комарци преку употреба на постелници, репеленти, итн Хемопрофилакса (види подолу), исто така може да се користи, особено кај патниците. Сепак хемиопрофилакса само потиснува паразитмија и не се спречи инфекцијата.
Контролните активности на ниво на заедницата може да се користат пристапи кои директно намали контакт со луѓе комарци, како и пристапи кои се намали вкупниот број на комарци во областа. Таквите пристапи вклучуваат намалување на комарците размножување (на пример, промена на животната средина), целни фази ларва со хемиски или биолошки агенси, и масовно инсектицид прскање за комарци за возрасни. Биолошки методи за контрола вклучуваат воведување на риби кои јадат ларви од комарци или бактерии (на пример, Bacillus thuringiensis) Кој излачуваат ларвите токсини. Откривање и лекување случај е уште еден потенцијален метод за контрола. Идентификување и лекување на заразените лица, особено асимптоматски лица, ќе ја намали големината на резервоарот за паразит во човечката популација и може да ја намали стапката на пренос. Сепак, ова може да биде релативно скапи пристап.
Овие пристапи не се исклучуваат и може да се комбинираат. Многу од успешните програми за контрола вклучуваат и мерки за контрола на комарците и третман на инфицирани лица. Не постои стандарден метод на контрола на маларијата која има докажано универзално ефективни. Епидемиолошки, социо-економски, културни и инфраструктурни фактори на одреден регион ќе се одреди најсоодветниот контрола на маларијата.Некои од факторите кои треба да се земат предвид се:
- инфраструктура на постоечките здравствени услуги и други ресурси
- интензитет и периодичност (на пример, сезонски) на пренос
- видови комарци (еколошки барања, карактеристики на однесувањето, инсектицид чувствителност, итн)
- паразит видови и дрога чувствителноста
- културни и социјални карактеристики на населението
- присуство на социјални и еколошки промени
Контрола на маларија во тропска Африка е особено проблематично, бидејќи на висока брзина на пренос и целокупната низок социо-економски план. Неколку студии покажале дека инсектицид третирани постелници (ITBN) намалување на морбидитетот и морталитетот поврзан со маларија. Во повеќето области на воведувањето на постелници не бараат големи промотивни програми и нивната употреба е лесно прифатени. Ова може да биде делумно се должи на намалувањето на непријатност комарци гризе. Некои прашања беа покренати во однос на економската одржливост на bednet програми. Тоа е потребно повторно да се третираат со инсектициди постелници периодично и постелници треба да се поправат и да се замени, како тие стануваат искинати и се истроши. Покрај тоа, некои ја зголемија загриженоста за долгорочните бенефиции на постелници бидејќи тие се намали изложеноста, но не го елиминира.
[Преглед на контрола на маларијата: РС Филипс (2001) Моментална состојба на маларија и потенцијал за контрола. Clin.Microbiol. Rev. 14: 208].
|
Е осомничен маларија кај лица со историја на се во ендемска област и презентирање на симптоми на маларија (види Клинички манифестации). Овие симптоми, особено во раните фази на инфекцијата, не се специфични и често се опишува како слични на грип. Како што болеста напредува, пациентот може да покажуваат зголемена слезина и/или црниот дроб и анемија. Дијагнозата се потврдува со микроскоп. Дебела крв тестови генерално се повеќе чувствителни за откривање на паразити, со оглед на тенок тестови се претпочита за идентификација видови.(Види крв фаза морфологија на плазмодиум видови.) Ако паразити не се наоѓаат на првиот тест на крвта се препорачува да се направат дополнителни тестови на секои 6-12 часа, онолку долго колку што 48 часа. Некаков дијагноза на P. фалципарум (бројни и исклучиво ѕвони фази) може да претставува медицински итни случаи, особено во не-имунолошки лице. Рапид immunochromatographic тестови (на пример, прачки) врз основа на откривање на антиген се исто така достапни (види преглед).
Хемотерапијата и отпорност на лековите
Неколку антималарични лекови се на располагање. Многу фактори се вклучени во одлучувањето најдобриот третман за маларија. Овие фактори вклучуваат паразит видови, сериозноста на болеста (на пр., Сложени), возраста на пациентот и имунолошкиот статус, подложност на паразитот на лекови (на пример, отпорност на лековите ), а цената и достапноста на лекови. Затоа, точната препораки често ќе се разликуваат според географски регион. Покрај тоа, на различни лекови дејствуваат различно на различни фази на животниот циклус (Табела). Други линкови на интерес:
- Механизми на дрога акција и Отпорот
- Виртуелна Поморска болница, информации за третман и против маларија
- СЗО, водич на анти-малярия користење
- Медицински член писмо на лекови за паразитски инфекции
Избрани антималарични лекови Класа дрога Примери Брзо дејство крв шизонoсид холерокин (+ други 4-аминохинолини), кинин, кинидин, мефлоквин, халофантрин, антифолати (пириметамин, прокунил, сулфадоксин, дапсон), артемизинин деривати (quinhaosu) Бавно дејствувачки крв шизонocide доксициклин (+ други тетрациклин антибиотици) Крв + ткиво шизонoсид блага прогванил, пириметамин, тетрациклини Ткиво шизонoсид (анти-повратна) примакаин Гаметоцидален примакаин, артемизинин деривати, 4-аминохинолини (ограничен?) Комбинации Фансидар (пириметамин + сулфадоксин), Малоприм (пириметамин + дапсон), Маларон (атовакване + прогванил) Брзо дејство крв шизонocides, кои дејствуваат на сцената на паразитот во крвта, се користат за лекување на акутни инфекции и брзо да се ослободат од клинички симптоми. Хлороквин е генерално се препорачува третман за пациенти со P. vivax, P. ovale, P. маларија, и некомплицирано хлорокин осетлива на P. фалципарум инфекции. Хлорокин е безбеден и обично добро се поднесува. Несакани ефекти може да вклучуваат пруритус (односно, чешање), гадење или агитација. Пациентите инфицирани со или P. vivax и P. ovale, и дека не се изложени на висок ризик за реинфекција, исто така, треба да се третира со примакаин (ткиво шизонocide). примакаин е ефикасен против фаза на црниот дроб на паразитот, вклучувајќи хипнозоитs (види рецидиви), и ќе се спречат идни релапси. Комбинацијата на хлорокин и примакаин често се нарекува “радикални лек”.
Тешка, или комплицирано, фалципарум маларија е сериозна болест со висока стапка на смртност и мора да се смета за опасна по живот, а со тоа и бара итно лекување. Третман обично бара парентерална администрација на лекови (на пример, инјекции) од пациентите често се во кома или повраќање, и на тој начин не може да се земе лекови усно. Парентерална формулации се достапни за хлорокин, кинин, хинидин и артемизинин деривати.деривати на артемизинин генерално се изборот, но се уште не се одобрени насекаде. На пример, во кинин САД и кинидин се одобрени лекови за тешка маларија. Пациентите треба да бидат постојано следени за хематокрит, паразитмија, нивото на хидратација, хипогликемија, и знаци на токсичност од лекови и други компликации во текот на лекувањето. Прекинувачот на орална администрација треба да се направи што е можно пациентот е во состојба. Најмногу смртни случаи се должи на тешка маларија се случи во или блиску до дома и во ситуации каде што пациентите не можат да се преземат во болница. Супозитории кои може да се примени од страна на селото здравствените работници, исто така, се развива и се покажа за да бидат безбедни и ефикасни.
Ефикасноста на хлорокин е значително намалена со широк отпор ширењето хлорокин на P. фалципарум и појавата на хлорокин отпорни P. vivax. Ако хлорокин терапија не е ефикасна, или ако во област со хлорокин отпорни на маларија, заеднички алтернативни третмани вклучуваат: мефлокин, кинин во комбинација со доксициклин или Fansidar®. Деривати на артемисинин (дихидроартемизинин, артесунате и артеметер) се повеќе се користи во Азија и Африка, а сега се препорачуваат како прва линија на третман од страна на Светската здравствена организација. Овие лекови првично биле добиени од растителни пелинот (Artemesia annua). И се користи за долго време во Кина, како билен чај quinhaosu повика да се третираат фебрилни болести. За да се спречи висока стапка повторно поврзани со артемисинин деривати и да го забави развојот на отпорност на лековите се препорачува третманот да се комбинираат со неповрзани против маларијата. Лекови кои се користат во комбинација со артемисинин вклучуваат мефлокин, лумефантрин, Fansidar® и амодијакин.
Хемиопрофилакса. Хемиопрофилакса е особено важно за лицата од не-маларични области кои го посетуваат области ендемични за маларија. Такви кои не се имуни лица можат брзо да се развие сериозна и опасна по живот болест. Како и во случај на третман не постои стандардна препорака и избори за хемиопрофилакса се многу зависни од условите поврзани со патување и индивидуално лице. (Види ЦДЦ лист за спречување на маларија.) Хемопрофилакса бара употреба на не-токсични лекови од овие лекови ќе се земе во текот на подолг временски период на време. Општо земено на пациентот ќе почне да се земе лек, пред да замине, а потоа продолжи земање на дрога за време на престојот во ендемски области и продолжи земање на дрога, по враќањето. Оваа е да се осигура на дрога се одржува на доволно ниво во текот на посетата и да се заштити од било која инфекција добиени за време на посетата. За жал, многу од ефикасни и не-токсични лекови (на пример, хлорокин, пириметамин, прогванил) имаат ограничена употреба, бидејќи на отпорност на лековите. Друга стратегија е најверојатниот (или ‘екранот во мирување’) третман да се користи во комбинација со профилакса. Во овој случај некое лице или се појави профилакса или го хлорокин или друг релативно не-токсични лекови за профилакса и носи дрога како Fansidar.
Употребата на мефлокин за маларија хемиопрофилакса е нешто контроверзно. Мефлокин е ефикасна во спречување на маларија со една прави неделно, со што се нуди предности на лекови кои треба да се внесува дневно. На оваа доза мефлокин се поднесува од страна на повеќето поединци. Сепак, некои луѓе имаат невропсихијатриски негативни влијанија како што се нарушувања на спиењето и ноќни кошмари. Ова може да се влошува од страна на меѓународно патување кое е стресна настан. Рандомизирани, заслепени и контролирани испитувања покажуваат дека невропсихијатриски негативни влијанија се само малку повисоки со мефлокин отколку со други анти-маларија.
Тепање на екзоэритроцит фаза (на пример, црниот дроб), ќе се спречи инфекција на крвта и е познат како причинско-последична профилакса. Ова е пожелно со тоа што го ограничува износот на време треба да се преземат пред профилактички лекови и по патувањето во ендемска област. Единствено во моментов на располагање лек за причинско-последична профилакса е примакаин. Сепак, маларија профилакса не е одобрена употреба на примакаин и треба да се препишува само за профилакса за еден од случај до случај. На пример, за лица кои често имаат патувања во кратко времетраење да се многу ендемични области и дека лицето не покажува недостаток на глукоза-6-фосфат дехидрогеназа. Тафенокин во моментов е во фаза на евалуација поле за неговата употреба во причинско-последична профилакса.
Осврти за третман на маларија:
- Pasvol G (2006) Третманот на комплицирана и тешка маларија. Br Мед Бул 75-76: 29-47 .
- Њутн P и бела Њу Џерси (1999) Маларија: новите случувања во лекување и превенција. Annu Rev Мед 50: 179.
- Белата Њу Џерси (1996) третирање на маларија. N Engl J Med 335: 800.
- Белата Њу Џерси (2008) Qinghaosu (Artemisinin): Цената на успех. Наука 320, 330-334 .
 Отпорност на лековите
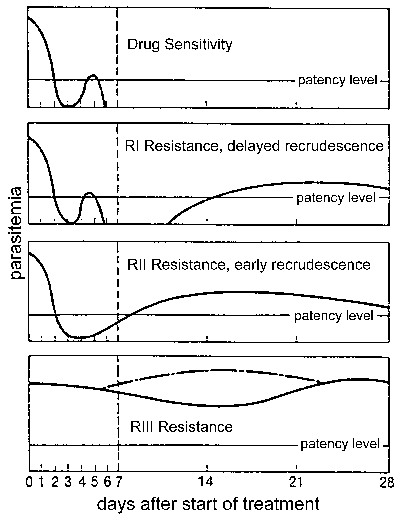
Отпорност на лековитеОтпорност на лековите, а особено, отпорност на хлорокин е голем здравствен проблем во контролата на маларијата.отпорност на лековите е дефинирана со прекин на третманот и може да се оценува во различни нивоа во зависност од времето на повторно по третманот (Слика). Традиционално овие нивоа на отпорност на лековите се дефинирани како чувствителни (без повторно), Р.И. (одложен повторно), RII (почетокот повторно) и RIII (минимални или никакви анти-паразит ефект). Модифициран протокол врз основа на клиничкиот исход беше воведен од страна на СЗО во 1996 година овој протокол на ниво на отпор се изразува како соодветен клинички одговор (ACR), кон крајот на неуспех на третманот (LTF), или почетокот на неуспех на третманот (ЕТФ) како што е дефинирано од страна на следниве:
- АЦР, отсуство на паразитмија (без оглед на треска) или отсуство на клинички симптоми (без оглед на паразитмија) на 14-тиот ден за следење
- LTF, повторно појавување на симптомите или присуство на паразитмија 4-14 дена за време на следење
- ЕТФ, упорноста на клинички симптоми, во присуство на паразитмија текот на првите 3 дена за следење
Или протокол може да се користи за одредување на отпорност на лековите, но протоколот клиничкиот исход е повеќе практични во области на интензивни пренос, каде што може да биде тешко да се направи разлика повторна инфекција од повторно и каде паразитмија во отсуство на клинички симптоми се чести. Отпорност на лековите од страна на или протокол се определува со ин виво тестови во кои пациентите се хоспитализирани и се следи за време и по стандарден третман со лекови. Исто така, постојат ин витро тестови кои може да се процени нивото на отпорност на лековите преку утврдување на ефикасноста на лекови против P.фалципарум одгледуваат во култура (види отпорноста на лековите: маларија на СЗО). In vivo и in vitro тестови не секогаш соодветствуваат од имунитетот на домаќинот и други фактори можат да влијаат на ин виво резултати.Идентификацијата на специфични мутации кои би можеле да бидат поврзани со отпорност на лековите (види Табела на другата страна), исто така може да доведе до развој на тестови врз основа на молекуларни маркери.
Отпорност на лековите се развива кога паразити со намалена чувствителност на антималарични лекови се избрани под притисок на дрога. Намалена чувствителност на дрога може да се доделат со неколку механизми (види механизми на отпорност на лековите). И се одразува генетска мутација (а) или полиморфизам во популација паразит. паразити на дрога отпор ќе имаат селективна предност во однос на чувствителни на лекови паразити во присуство на дрога и ќе бидат првенствено пренесуваат. Главни фактори во развојот на отпорност на лековите се употребата на субтерапевтски дози на лекови или не завршување на терапискиот режим (Табела). На пониските нивоа на дрога ќе се елиминираат најмногу подложни паразити, но и оние кои можат да го толерираат лекот ќе се опорави и да го репродуцираат. Со текот на времето тоа ќе доведе до континуирана избор за паразити кои може да се толерира, дури и повисоки дози на лекот. Тоа е од клучно значење за одржување на адекватно концентрацијата на лекот за доволно време за целосно да се елиминира паразити од која било дадена индивидуа.
Фактори кои придонесуваат за развој
и ширење на отпорност на лековитеФактор Коментари Само-лекување Поединци може да се земе само на дрога додека симптомите се јасни или ќе се пониски дози за да заштедат пари. Сиромашните усогласеност Поединци не може да заврши на полно разбира на третман, бидејќи на дрога несакани ефекти. Маса администрација Широката употреба на дрога во областа на интензивна трансмисија зголемува притисокот дрога со изложување поголем паразит населението на дрога. Долго дрога полуживот Лекови кои се елиминираат полека ќе доведе до повеќе изложеност на паразитот да субтерапевтски концентрации на лекот. Интензитетот на пренос Високо ниво на пренос може да се овозможи повторна инфекција додека лекови се на под-терапевтски нивоа. Отпорност хлорокин. По неговото воведување во близина на крајот на Втората светска војна, хлорокин брзо стана лек на избор за третман и превенција на маларија на. Не само што е хлорокин ефикасен лек, веројатно се должи на неговата страница на дејствување во вакуола храна и нејзиното мешање со формирање хемозоин (види дејството на лекот), туку тоа исто така е релативно не-токсични и евтини. Две жаришта на отпорни хлорокин P. фалципарум беа откриени во Колумбија и на границата на Камбоџа, Тајланд, во текот на доцните 1950-тите. Во текот на 1960-тите и 1970-тите, отпорни на паразити се шири низ Јужна Америка, Југоисточна Азија и Индија. Отпорот беше прв објави во источна Африка во 1978 година и се шири низ целиот континент во текот на 1980-тите. Хлороквин отпорни на P. vivax не бил пријавен до 1989 година во Папуа Нова Гвинеја, а сега се најде во неколку жаришта во југоисточна Азија, а можеби и Јужна Америка.
Основата на отпорот хлорокин се намалува акумулацијата хлорокин во храната вакуола на паразитот. Исто така, отпорност на хлорокин делумно може да се промени со инхибитори на P-гликопротеин (на ABC превозник) кои се одговорни за мулти-отпорност на лековите (МДР) во туморските клетки линии, со што се укажува на ваквата појава може да се случи во плазмодиум. Мутации во MDR-како ген од P. фалципарум (Pf mdr1) беа вмешани во отпор хлорокин. Сепак, овие мутации не се предвидливо на отпор хлорокин во сите географски области. Pf MDR1 чини да се придонесе за степен на отпорност на хлорокин, но само тоа не е доволно да се состане на отпорот. Сепак, PfMDR1 се појави да играат улога во отпорот на мефлокин и халофантрин и влијае на чувствителност на артемисинин.
Уште еден кандидат за генетски локус на отпор хлорокин беше идентификуван преку генетска крст и мапирање експеримент. Е пронајдена 400 kb регионот на хромозомот 7 да се изолирам со отпор хлорокин и понатамошна анализа сугерира дека еден ген, наречен Pf CRT, беше одговорен за отпор хлорокин. Од вкупно 10 полиморфизми идентификувани во овој ген, само еден мутација е perfectedly поврзани со фенотип отпорот хлорокин. Оваа мутација резултира со лизин во остаток 76 се менува на треонин (K76T). Неколку теренски истражувања покажале поврзаност помеѓу Pf CRT-K76T и хлорокин отпор со користење на двете in vivo и in vitro методи. Тоа е неодамна сугерираше дека имало најмалку 4 основач мутации во Pf ген CRT поврзани со различни географски региони: Азија/Африка, Папуа Нова Гвинеја, Бразил/Перу и Колумбија (Wootton et al, Природа 418: 320, 2002). Се претпоставува дека употребата на хлорокин резултираше со следните избор и се шири на отпорни фенотип.
Критика на отпорност на лековите:
- Боланд ФБ (2001) отпорност на лековите во маларија. WHO / CDS / CSR / ДРС / 2.001,4
- Хајд JE (2007) дрога отпорни на маларија – увид. FEBS весник 274, 4688-4698 .
- Warhust D (2001) Нови градби: хлорокин отпор во плазмодиум фалципарум . Отпорност на лековите Новости 4: 141.
- Wellems ТЕ и Plowe CV (2001) Хлороквин отпорни на маларија. J Inf Dis 184: 770.
- Wongsrichanalai C, Pickard AL, Wernsdorfer WH и Meshnick SR (2002) Епидемиологија на дрога отпорни на маларија. Lancet зарази Dis 2: 209.